Razširjeni povzetek
Povzeti pregledni članek avtorjev Holst in Landolt (2018) na jasen in poglobljen način predstavlja trenutno razumevanje kemijskih mehanizmov, ki uravnavajo spanje in budnost pri ljudeh. Avtorja sta strnila znanstvena spoznanja iz raziskav na živalih in ljudeh ter uporabo novih metod, kot je optogenetika, ki ponujajo uvid v to, kako različne snovi v možganih vplivajo na budnost in spanec. Poudarjata, da spanje in budnost nista pasivna procesa, ampak dinamični stanji, ki ju ureja zapletena mreža kemičnih signalov.
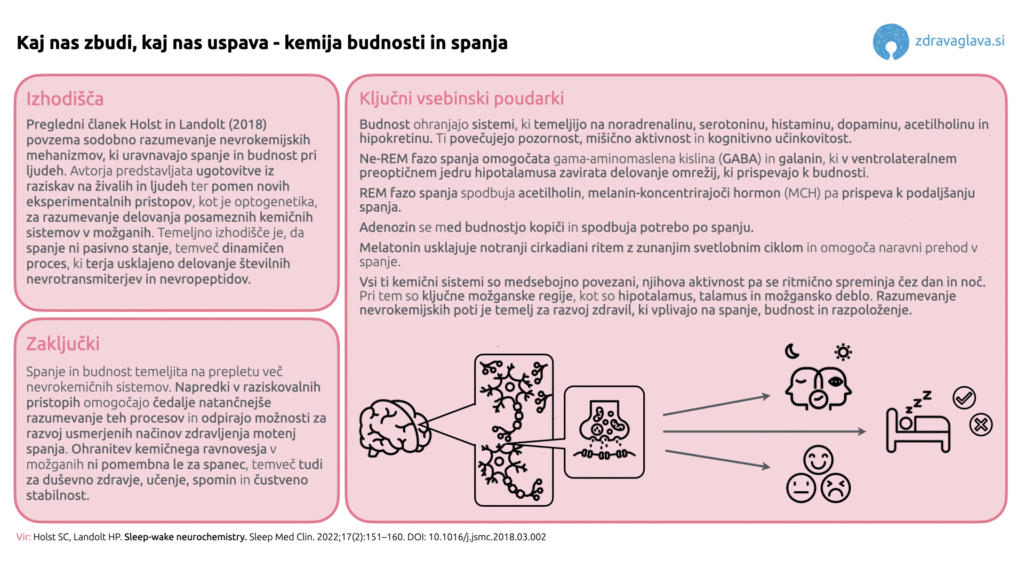
V nadzor nad budnostjo in spanjemi je vključenih veliko klasičnih nevrotransmiterjev, kot so dopamin, serotonin, noradrenalin, acetilholin, in nevropeptidov (v primerjavi s klasičnimi nevrotransmiterji so to večje molekule, ki se izločajo in učinkujejo počasneje in predvsem uravnavajo delovanje nevronov in sinaps (npr. hipokretin, melanin-koncentrirajoči hormon).
- Budnost uravnavajo predvsem noradrenalin, serotonin, histamin, dopamin, acetilholin in hipokretin. Te snovi delujejo v različnih delih možganov, kot so možganska skorja (vključno z bazalnim delom njenega čelnega režnja), hipotalamus, in talamus, ter spodbujajo pozornost, mišično aktivnost in kognicijo.
- Spanje, predvsem ne-REM fazo, podpirajo snovi, kot sta GABA in galanin, ki “ugasnejo” budilne centre v možganih. Ključna regija za spanje je t.i. ventrolateralno preoptično jedro (VLPO), kjer GABA in galanin zavirata sisteme, ki prispevajo k vzdramljenosti. REM spanje spodbuja acetilholin, medtem ko melanin-koncentrirajoči hormon (MCH) prispeva k podaljšanju spanja in zmanjšanju budnosti.
- Adenozin je snov, ki se čez dan kopiči in s tem spodbuja potrebo po spanju. Ko smo dlje časa budni, raven adenozina v možganih raste, kar nas postopoma utrudi. Kofein k povečani budnosti prispeva tako, da deluje kot antagonist adenozinskih receptorjev.
- Melatonin usklajuje notranji čas telesa s ciklom dneva in noči. Njegovo sproščanje se v temi poveča, kar telesu sporoči, da se pripravlja na počitek, medtem ko svetloba ta proces zavre. Deluje kot regulator ritma spanja, ne kot uspavalno sredstvo in omogoča, da se fiziološki procesi uskladijo z nočnim obdobjem in tako podprejo naravni prehod v spanec.
Avtorja izpostavljata, da se delovanje naštetih snovi ne izključuje, temveč dopolnjuje v prepletenih omrežjih, kjer se njihova aktivnost dinamično spreminja skozi dan in noč. Vloga hipotalamusa, možganskega debla in talamusa kot središč za usklajevanje teh procesov je ključna.
Razumevanje te zapletene kemične regulacije je pomembno za diagnosticiranje in zdravljenje številnih težav s spanjem, saj lahko motnje v delovanju teh kemičnih poti vodijo do nespečnosti, prekomerne dnevne zaspanosti, narkolepsije, motenj cirkadianega ritma ali težav pri vzdrževanju kakovostnega spanca. Številna zdravila za spanje ali budnost ciljajo prav na te kemične poti, npr. uspavala delujejo na GABA receptorje, kofein zavira adenozinske, antidepresivi vplivajo na serotonin, stimulanti pa povečajo raven dopamina in noradrenalina.
Avtorja zaključujeta, da spanje in budnost uravnava več soodvisnih kemičnih sistemov in možganskih omrežij. Te procese je možno natančno preučevati z novimi znanstvenimi metodami, kar lahko v prihodnje vodi do boljšega razumevanja in učinkovitejših zdravljenj motenj spanja. Posebej izpostavita, da ravnovesje med temi kemičnimi snovmi ni samo ključno za dober spanec, temveč tudi za splošno duševno zdravje, učenje, spomin in čustveno uravnavanje.
Povzela: Liza Rozman, MSc iz kognitivne nevroznanosti
Bibliografski podatki o objavi
- Holst SC, Landolt HP. Sleep-wake neurochemistry. Sleep Med Clin. 2022;17(2):151–160. DOI: 10.1016/j.jsmc.2018.03.002